Je dovolené hrať sa na Boha?
DR. Andrea Bannert je v spoločnosti od roku 2013. Doktor biológie a medicíny, redaktor, najskôr vykonával výskum v mikrobiológii a je odborníkom tímu na malé veci: baktérie, vírusy, molekuly a gény. Pracuje tiež na voľnej nohe pre Bayerischer Rundfunk a rôzne vedecké časopisy a píše fantasy romány a príbehy pre deti.
Viac o expertoch na Všetok obsahu kontrolujú lekárski novinári.Prvýkrát sa podarilo úspešne opraviť genetickú zmenu v ľudských embryách. Technológiou sa však dajú liečiť nielen choroby. Farba očí a ďalšie vlastnosti by mohli byť tiež vopred určené týmto spôsobom. Bude návrhárske dieťa čoskoro?
Simon K. * pri cvičení skolaboval a už sa viac nezobudil. Diagnóza: náhla srdcová smrť. Mladý atletický muž trpel takzvanou hypertrofickou kardiomyopatiou alebo skrátene HCM. Pri tejto chorobe dochádza k zahusteniu tkaniva srdcového svalu v ľavej komore. Porucha je pomerne častá. Každý z 500 ľudí je postihnutý a mnohí na to zomrú.
Nožnice hľadajú vodcov
Zvláštnosť HCM: Informácie, takzvaný genetický kód, sa menia iba v jednom bode vo veľmi špecifickom géne. Vedci tomu hovoria mutácia. Existuje približne 10 000 ďalších dedičných chorôb, ktoré sú vyvolané podobne izolovanými mutáciami. Cystická fibróza alebo kosáčikovitá anémia - dve rovnako život ohrozujúce choroby. Zjavnou myšlienkou je opraviť vážne genetické chyby čo najskôr.
Donedávna nemožné úsilie. Vedci poznajú enzýmy, ktoré môžu „rezať“ DNA, ale tieto molekuly bielkovín nehovoria rovnakým jazykom ako genetické informácie. Preto nedokážu vystopovať defekt v genóme.
To sa zmenilo veľkolepým objavom dvoch vedcov Jennifer Doudna a Emmanuelle Charpentier pred štyrmi rokmi. Náhodou našli v baktériách enzým, ktorý môže prerezať reťazce DNA a niesť so sebou malý úlomok genetického materiálu ako tlmočník. Dokáže prečítať obrovské množstvo údajov v DNA a navádza molekulárne nožnice presne tam, kde majú strihať. Vedci pomenovali účinný tím „CRISPR / Cas9“ - baktérie ho potrebujú na obranu pred vírusmi.
Dedičná choroba štípala v zárodku
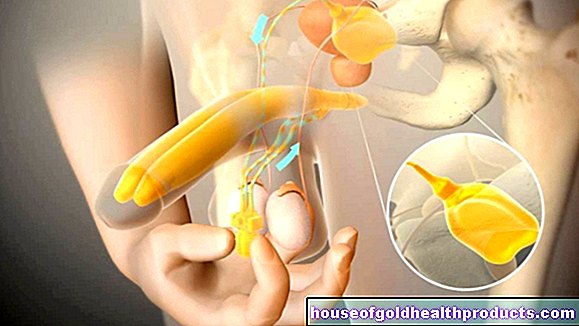
Skupina vedcov z Oregonskej univerzity zdravia a vedy v Portlande použila génové nožnice na vymazanie hypertrofickej kardiomyopatie veľmi skoro v genetickom kóde - v embryách. Tím Shoukhrata Mitalipova vybavil nožnice na gén genetickou sekvenciou, ktorá rozpoznáva presné umiestnenie v DNA, v ktorej je choroba naprogramovaná.
Svoj nový super nástroj použili na 58 embryí, ktoré boli vytvorené zo spermií muža trpiaceho HCM a vaječných buniek zdravej ženy. Také pokusy sú možné v USA. V Nemecku však zákon o ochrane embryí bráni použitiu ľudských embryí na výskumné účely.
Senzačná úspešnosť
Americký experiment fungoval: úryvok „tlmočníka“ naviedol molekulárne nožnice Cas9 presne k zmutovanému segmentu DNA a oddelil ho. Teraz vlastné opravné mechanizmy bunky boli schopné obnoviť gén.
Úspech dokonca ohromil aj samotných vedcov: patogénna mutácia zmizla v 42 embryách - úspešnosť 72 percent.
„V bunkových kultúrach však CRISPR / Cas9 dlho nefungoval tak dobre ako v živých embryách,“ hovorí Jun Wu, jeden z autorov štúdie. Vedci sa domnievajú, že dôvodom sú obzvlášť dobre fungujúce stroje na opravu DNA v raných embryonálnych štádiách.
Predchádzajúci experiment čínskych vedcov v apríli 2015 fungoval výrazne horšie ako experiment amerických vedcov. Na rozdiel od Mitalipova a jeho tímu Číňania pridali génové nožnice do oplodneného vajíčka iba pomocou svojho tlmočníka - a nie v čase oplodnenia.
Nožnice sa vymkli spod kontroly
A čínski vedci museli zápasiť s ďalším problémom, s ktorým sa Mitalipovov experiment nestretol: takzvanými mutáciami mimo cieľa. Sú považované za najväčšie nebezpečenstvo pri použití CRISPR / Cas9.
Mimo cieľa znamená, že nožnice na gény sa strihajú aj na iných miestach, ako je požadované. A nie všetko sa dá správne dať dohromady vlastnými opravami bunky. Potom vzniknú nové mutácie, ktoré by mohli napríklad spôsobiť rakovinu.
„Jazdíme na aute, ktoré stále staviame.“
Mitalipov a jeho kolegovia svojim pokusom obnovili etickú diskusiu o tom, či je ľuďom dovolené manipulovať s embryami. V Nemecku je zatiaľ povolená iba takzvaná preimplantačná diagnostika. Zahŕňa to vyšetrenie genetického materiálu embryí po umelom oplodnení mimo maternice a použitie iba zdravých embryí - t. J. Tých, ktoré nenesú závažné dedičné ochorenie, akým je napríklad HCM. A metódu je možné vôbec použiť iba vtedy, ak hrozí vážne dedičné ochorenie.
Technika CRISPR / Cas9 môže tiež vyliečiť tie embryá, ktoré by boli vybrané počas preimplantačnej diagnostiky. Teoreticky Pretože či je to naozaj lepšie, to sa ešte uvidí. Riziká spojené s liečbou génovými nožnicami zatiaľ nemožno s konečnou platnosťou posúdiť - vedci sa na tom zhodujú. Jacob Corn, riaditeľ iniciatívy Genomics na Kalifornskej univerzite v Berkeley, o stave výskumu CRISPR / Cas9 povedal: „Riadime auto, ktoré stále staviame.“
Neznáme nebezpečenstvá
Jedenásť veľkých amerických vedeckých organizácií požaduje v American Journal of Human Genetics „opatrný, ale angažovaný prístup“. Kým neviete, či výhody skutočne prevažujú nad rizikami. Vedci preto považujú za „v súčasnosti nevhodné“ vloženie geneticky modifikovaného embrya od ženy a vyvolanie tehotenstva.
Embryá CRISPR / Cas z Mitalipovovho experimentu boli zničené po niekoľkých dňoch. V tomto čase sa embryo skladá z malého, tekutinou vyplneného bunkového balónika, blastocysty. Vedci zatiaľ nedefinujú toto embryonálne štádium ako ľudský život. Ak sa blastocysta neimplementuje do maternice, v laboratóriu sa z nej vytvoria „iba“ embryonálne kmeňové bunky.
Otázku, kedy život začína, je možné samozrejme polemizovať. Napríklad v Nemecku môžu byť embryá zmrazené iba v takzvanom pronukleárnom štádiu a na účely umelého oplodnenia a v určitom okamihu zničené. Pri nich sa jadro vaječnej bunky ešte úplne nespojilo so spermou. Mnoho vedcov požaduje, aby sa takéto štruktúry používali na ciele výskumu na vysokej úrovni.
Dizajnérske deti?
Ako ďaleko však môžete zájsť v genetickom výskume a terapii? Objaviteľ CRISPR / Cas9 Doudna má obavy a hovorí: „Často som sa sám seba pýtal, čo by výskumníci urobili s touto technológiou, za existenciu ktorej som čiastočne zodpovedný.“ Možno by vytvorili dizajnérske dieťa, o ktorom by rodičia rozhodovali nielen o zdraví. , ale tiež určiť farbu vlasov, farbu očí, inteligenciu a povahu - ak takémuto experimentu vopred nebráni zákon. Je najvyšší čas určiť, aké riziká môžu výskumníci podstúpiť pri genetickej úprave embryí a ktoré manipulácie by mali byť v zásade zakázané.
* Názov zmenil redaktor.
Tagy: stres zubná starostlivosť nemocnica